Άγγελος Κραμβής1, Αμαλία Παπανικολάου1, Αναστάσιος Αποστολός1,2, Δαβίδ-Δημήτρης Χλωρογιάννης3, Μαρία Μποζίκα1, Κασσιανή Μαρία Ναστούλη1, Φίλιππος Τιμπιλής1, Αθανασία- Μαρία Γεώργα1, Αναστασία Λάττα1, Δήμητρα Τζέγκα1, Κορνηλία Πέπα1, Φώτης Καλλίνικος1, Μιχαέλα Ρούτουλα1, Στέλλα Ρούζη1, Βασιλική Φωτοπούλου1, Αντώνιος Καρανάσος1, Μιχαήλ Ι. Παπαφάκλης1, Περικλής Νταβλούρος1, Γρηγόριος Τσίγκας1
1 Τμήμα Καρδιολογίας, Πανεπιστημιακό Νοσοκομείο Πατρών, Πάτρα, Ελλάδα
2 Πρώτη Καρδιολογική Κλινική, Γενικό Νοσοκομείο Ιπποκράτειο, Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών, Αθήνα, Ελλάδα
3 Τμήμα Ακτινολογίας, Νοσοκομείο Brigham and Women’s, Βοστώνη, ΜΑ 02115, ΗΠΑ
Περίληψη
Η βέλτιστη διάρκεια της διπλής αντιαιμοπεταλιακής αγωγής (ΔΑΜΑ) μετά από διαδερμική στεφανιαία παρέμβαση (PCI) παραμένει αντικείμενο εκτεταμένης συζήτησης και έρευνας. Η παρούσα ανασκόπηση εξετάζει το σκεπτικό για μείωση της διάρκειας της ΔΑΜΑ σε συγκεκριμένους πληθυσμούς. Συζητάμε τις προκλήσεις που σχετίζονται με την επίτευξη της χρυσής ισορροπίας μεταξύ των ισχαιμικών και αιμορραγικών κινδύνων σε ασθενείς που υποβάλλονται σε PCI, υπογραμμίζοντας τη σημασία των προσαρμοσμένων θεραπευτικών προσεγγίσεων με βάση εξατομικευμένα προφίλ κινδύνου. Επιπλέον, εστιάζουμε στα στοιχεία που υποστηρίζουν τη συντομευμένη ΔΑΜΑ σε ομάδες ασθενών υψηλού κινδύνου, συμπεριλαμβανομένων εκείνων με αυξημένο αιμορραγικό κίνδυνο, συνυπάρχουσες κακοήθειες, σακχαρώδη διαβήτη και σύνθετη στεφανιαία νόσο. Τα αναδυόμενα δεδομένα υποδηλώνουν ότι τα συντομευμένα σχήματα ΔΑΜΑ προσφέρουν συγκρίσιμα αποτελεσματα στην πρόληψη των θρομβωτικών συμβάντων, μειώνοντας παράλληλα τις αιμορραγικές επιπλοκές.
Εισαγωγή
Η χορήγηση αντιαιμοπεταλιακής αγωγής αποτελεί κομβικό σημείο για την διαχείριση των ασθενών που υποβάλλονται σε διαδερμική στεφανιαία παρέμβαση (PCI) για Χρόνια Στεφανιαία Σύνδρομα (ΧΣΣ) ή Οξέα Στεφανιαία Σύνδρομα (ΟΣΣ). Ως στόχο έχει την πρόληψη της θρόμβωσης της ενδοπρόθεσης, της επαναστένωσης και των ανεπιθύμητων συμβάντων, όπως το έμφραγμα του μυοκαρδίου ή το ισχαιμικό εγκεφαλικό επεισόδιο. Οι βέλτιστες θεραπευτικές στρατηγικές, συμπεριλαμβανομένης της επιλογής, του συνδυασμού, του χρονισμού και της διάρκειας της θεραπείας, απαιτούν σχολαστική αξιολόγηση πολλαπλων παραγόντων. Οι θεραπευτικές αποφάσεις πρέπει να εξισορροπούν προσεκτικά τα οφέλη της αντιθρομβωτικής θεραπείας με το ενδεχόμενο σοβαρής ή/και απειλητικής για τη ζωή αιμορραγίας (1).
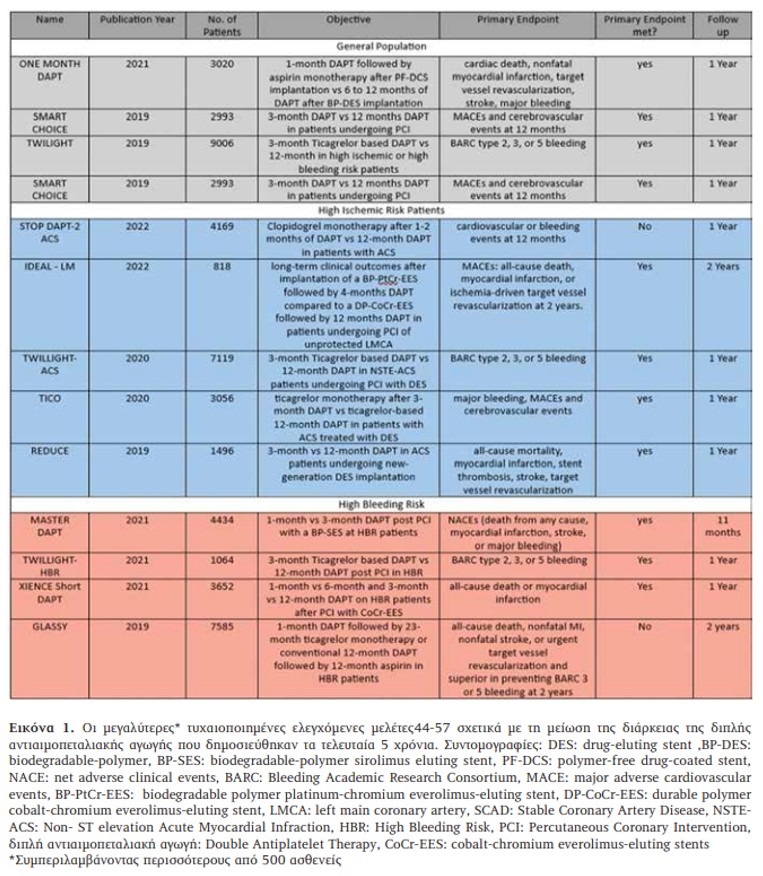
Σύμφωνα με τις τρέχουσες κατευθυντήριες οδηγίες της Ευρωπαϊκής Καρδιολογικής Εταιρείας (ESC), η διπλή αντιαιμοπεταλιακή αγωγή συνιστάται ως πρότυπο για 6 μήνες για ασθενείς με ΧΣΣ και για 12 μήνες μετά από ΟΣΣ. Ωστόσο, η διάρκεια αυτή δύναται να παραταθεί για ασθενείς υψηλού ισχαιμικού κινδύνου και να συντομευθεί για ασθενείς με υψηλό κίνδυνο αιμορραγίας (2-3). Στην Εικόνα 1 συνοψίζονται Πολυάριθμες Τυχαιοποιημένες Ελεγχόμενες Μελέτες (RCT) και μετα-αναλύσεις που έχουν προτείνει εναλλακτικές θεραπευτικές προσεγγίσεις για ασθενείς με ΧΣΣ ή ΟΣΣ. Οι προτάσεις αυτές εστιαζουν στη μείωση της διάρκειας της ΔΑΜΑ σε 1-3 ή 3-6 μήνες μετά την PCI και τη μετάβαση σε μονοθεραπεία P2Y12 ως μορφή αποκλιμάκωσης (4). Η παρούσα μελέτη αποσκοπεί σε μια ολοκληρωμένη επισκόπηση των υφιστάμενων στοιχείων σχετικά με τη συντομευμένη διάρκεια ΔΑΜΑ, με έμφαση στη διαχείριση ασθενών με συγκεκριμένες συννοσηρότητες, ανατομικά και τεχνικά ζητήματα κατά τη διάρκεια της PCI.
Η σημασία του συντομευμένου μοντέλου της ΔΑΜΑ.
Οι συνεχιζόμενες εξελίξεις στις τεχνολογίες των stent, σε συνδυασμό με την εισαγωγή νέων αντιαιμοπεταλιακών παραγόντων, ώστε να συμπεριληφθεί ένας γηράσκων και ιατρικά πολύπλοκος πληθυσμός με ανατομικά περίπλοκη στεφανιαία νόσο (CAD), παρουσιάζουν αξιοσημείωτες προκλήσεις στη διαχείριση των ασθενών που υποβάλλονται σε διαδερμικές στεφανιαίες επεμβάσεις (5).
Η λεπτή ισορροπία μεταξύ των παραγόντων υψηλού κινδύνου για αιμορραγία και θρόμβωση συνιστά ένα καθημερινό κλινικό δίλημμα. Τόσο ο θρομβωτικός όσο και ο αιμορραγικός κίνδυνος είναι υψηλότεροι κατά τους πρώτους μήνες μετά την PCI. Στη συνέχεια, μειώνονται και παραμένουν σχετικά σταθεροί με την πάροδο του χρόνου (6). Επιπλέον, η μείζων αιμορραγία επηρεάζει τη θνησιμότητα σε συγκρίσιμο ή και μεγαλύτερο βαθμό από τα μείζονα ισχαιμικά επεισόδια. Από την άλλη πλευρά, τα επεισόδια ελάσσονος αιμορραγίας μπορεί να οδηγήσουν σε απρόσμενη διακοπή της αντιαιμοπεταλιακής θεραπείας και εν δυνάμει αυξημένη εμφάνιση ισχαιμικών συμβαμάτων. Ως εκ τούτου, οι ασθενείς με υψηλό αιμορραγικό κίνδυνο μπορεί να ωφεληθούν από την τροποποίηση, είτε του συνδυασμού φαρμάκων, είτε της διάρκειας της ΔΑΜΑ. Μεταξύ των στρατηγικών που διερευνήθηκαν για τον μετριασμό των αιμορραγικών επεισοδίων, η μείωση της διάρκειας της ΔΑΜΑ ήταν η περισσότερο μελετημένη προσέγγιση (7) .
Ένα άλλο ζήτημα στο οποίο μπορεί να συμβάλλει θετικά η μείωση της διάρκειας της ΔΑΜΑ είναι η συμμόρφωση των ασθενών στα μακροχρόνια φαρμακευτικά σχήματα. Τα ποσοστά μη συμμόρφωσης των ασθενών μετά από έμφραγμα του μυοκαρδίου κυμαίνονται από 13% έως 60% για τις συνιστάμενες φαρμακευτικές αγωγές (8) . Η μη συμμόρφωση στη ΔΑΜΑ, ως στρατηγική δευτερογενούς πρόληψης, μετά από διαδερμική στεφανιαία παρέμβαση έχει αναφερθεί ότι αποτελεί τον ισχυρότερο ανεξάρτητο προγνωστικό παράγοντα για θρόμβωση της ενδοπρόθεσης (9), καθώς έχει καταδειχθεί τετραπλάσια συχνότητα εμφάνισης υποτροπιάζοντος συμβάντος (11,0% έναντι 2,8%; P=0,044) και διπλάσια συχνότητα νοσηλείας (21,2% έναντι 9,9%; P=0,04). Η πρόωρη διακοπή της διπλής αντιαιμοπεταλιακής αγωγής μπορεί να καθορίζεται όχι μόνο από τις ανεπιθύμητες ενέργειες των φαρμάκων, όπως η αιμορραγία, η δύσπνοια ή τα γαστρεντερικά συμπτώματα, αλλά και από ψυχολογικούς παράγοντες, όπως η κατάθλιψη και το άγχος, οι οποίοι θα μπορούσαν ενδεχομένως να συνδέονται με τις επιπλοκές που σχετίζονται με τη στεφανιαία νόσο (10-11).
Τέλος, η συντομευμένη ΔΑΜΑ μπορεί να μειώσει τη διάρκεια της πολυφαρμακευτικής αγωγής, μια πολύ συχνή κατάσταση για τα άτομα που πάσχουν από CAD, διότι εκτός από τα πολλαπλά φάρμακα που είναι απαραίτητα για τη δευτερογενή πρόληψη, όπως αντιαιμοπεταλιακά, αντιυπερτασικά, υπολιπιδαιμικά φάρμακα κ.λπ. πολλοί από αυτούς τους ασθενείς πάσχουν ταυτόχρονα από πρόσθετες συννοσηρότητες. Εκτός από το εκτεταμένο κόστος σε όλα τα συστήματα υγειονομικής περίθαλψης, η πολυφαρμακία αυξάνει την πιθανότητα ακατάλληλης χρήσης φαρμάκων και συνδέεται με υψηλότερα ποσοστά νοσηλείας και θνησιμότητας (12).
Τρέχοντα στοιχεία που υποστηρίζουν τη μειωμένη διάρκεια ΔΑΜΑ.
A. Γενικός πληθυσμός
Η ανάπτυξη των νεότερων γενεών ενδοπροθέσεων με έκλυση φαρμάκου (Drug Eluting Stents – DES) έχει οδηγήσει σε μειωμένα ποσοστά θρόμβωσης stent, διατηρώντας παράλληλα χαμηλά ποσοστά επαναστένωσης. Επιπλέον, οι πιο ισχυροί αναστολείς P2Y12, όπως η πρασουγρέλη και η τικαγρελόρη, προσφέρουν τη δυνατότητα χρησιμοποίησης τους ως μονοθεραπεία. Επιπλέον, η χρήση της ενδοαγγειακής απεικόνισης έχει συμβάλλει καθοριστικά στην βελτίωση των αποτελεσμάτων της αγγειοπλαστικής (13).
Κατά συνέπεια, αρκετές τυχαιοποιημένες ελεγχόμενες δοκιμές (RCTs) έχουν πραγματοποιηθεί για την αξιολόγηση της ασφάλειας της μειωμένης διάρκειας ΔΑΜΑ σε σύγκριση με τα μέχρι πρότινος δεδομένα. Πρόσφατα, διάφορες μετα-αναλύσεις των δημοφιλέστερων δημοσιευμένων RCTs, συγκρίνουν τη συντομευμένη (1-3 μήνες) ΔΑΜΑ με την τυπικής διάρκειας (6-12 μήνες) ΔΑΜΑ σε ασθενείς που υποβάλλονται σε διαδερμική στεφανιαία παρέμβαση με DES, τόσο για οξέα όσο και για χρόνια στεφανιαία σύνδρομα. Όλες κατέληξαν στο συμπέρασμα ότι η ΔΑΜΑ διάρκειας 1-3 μηνών μειώνει τα περιστατικά μείζονως αιμορραγίας χωρίς να αυξάνει τα ισχαιμικά συμβάντα σε σύγκριση με τη μεγαλύτερης διάρκειας ΔΑΜΑ. Ωστόσο, απαιτείται περαιτέρω διερεύνηση για τον προσδιορισμό του βέλτιστου αντιαιμοπεταλιακού παράγοντα μετά από 1-3 μήνες DAPT (14-16). Ο σωστός εντοπισμός και η διαστρωμάτωση κινδύνου των ασθενών με χαρακτηριστικά υψηλού ισχαιμικού ή υψηλού αιμορραγικού κινδύνου είναι θεμελιώδους σημασίας, καθώς αυτή η υποομάδα ασθενών μπορεί να επωφεληθεί περισσότερο από την προσαρμοσμένη ΔΑΜΑ.
B. Συντόμευση της ΔΑΜΑ σε ασθενείς με αυξημένο αιμορραγικό κίνδυνο.
Στην καθ’ ήμερα κλινική πράξη, εως και το 40% των ατόμων που υποβάλλονται σε διαδερμική στεφανιαία παρέμβαση ταξινομούνται ως ασθενείς με υψηλό αιμορραγικό κίνδυνο (HBR). Ωστόσο, αυτός ο ιδιαίτερος πληθυσμός συχνά εξαιρείται ή εκπροσωπείται ανεπαρκώς στις μελέτες που αφορούν τη διαχείριση των ασθενών μετά την PCI (17). Πρόσφατα, η Academic Research Consortium for High Bleeding Risk (ARC- HBR) ανέπτυξε έναν καθολικά αποδεκτό ορισμό για τους ασθενείς με υψηλό αιμορραγικό κίνδυνο με βάση τα δημοσιευμένα στοιχεία (18). Οι παράγοντες που σχετίζονται με αυξημένο αιμορραγικό κίνδυνο περιλαμβάνουν: ηλικία άνω των 75 ετών, χρόνια νεφρική νόσο, χρήση αντιπηκτικής αγωγής από το στόμα, αναιμία, μέτρια θρομβοπενία, κίρρωση ήπατος με πυλαία υπέρταση, ενεργό κακοήθεια, χρόνια αιμορραγική διάθεση, αυτόματη αιμορραγία που απαιτεί νοσηλεία ή μετάγγιση, ενδοκράνια αιμορραγία, μακροχρόνια χρήση ΜΣΑΦ από το στόμα ή στεροειδών, πρόσφατη μείζονα χειρουργική επέμβαση ή χειρουργική επέμβαση υπό ΔΑΜΑ.
Σε ασθενείς με τέτοια χαρακτηριστικά, δεδομένου ότι τα stent νέας γενιάς υφίστανται ταχύτερη ενδοθηλιοποίηση, η παράταση της ΔΑΜΑ πέραν των 1-3 μήνων μπορεί να είναι περιττή (19). Πρόσφατα, οι Costa et al. σε μια μετα-ανάλυση 11 μελετών και 9006 ασθενών συνέκριναν τα αποτελέσματα της πολύ σύντομης (1 μήνας) ή σύντομης (3 μήνες) με την τυπική (≥6 μήνες) διάρκεια της ΔΑΜΑ σε HBR ασθενείς. Η συντομευμένη ΔΑΜΑ μείωσε τα μείζονα αιμορραγικά φαινόμενα (RR: 0,80, 95% CI: 0,64-0,99, I2 = 0%) και την καρδιαγγειακή θνησιμότητα (RR: 0,79, 95% CI: 0,65-0,95, I2 = 0%) σε σύγκριση με την κλασσική ΔΑΜΑ. Επιπλέον, δεν παρατηρήθηκε καμία διαφορά στην ολική θνησιμότητα, στα μείζονα ανεπιθύμητα καρδιαγγειακά συμβάματα, στο έμφραγμα του μυοκαρδίου ή στη θρόμβωση του stent(20). Τα ευρήματα αυτά ενισχύουν την ασφάλεια και την αποτελεσματικότητα της συντομευμένης ΔΑΜΑ σε ασθενείς που ταξινομούνται ως υψηλού αιμορραγικού κινδύνου, συνηγορώντας υπέρ της ένταξής της στην φαρέτρα των θεραπευτικών στρατηγικών.
C. Συντόμευση της ΔΑΜΑ σε ασθενείς με αυξημένο κίνδυνο ισχαιμίας
Οι πρόσφατες κατευθυντήριες οδηγίες της ESC προτείνουν έναν ορισμό για τους ασθενείς με υψηλό ή μέτριο θρομβωτικό κίνδυνο. Σκοπός αυτού, είναι η διαστρωμάτωση του κινδύνου, αλλά και ο καθορισμός της αντιθρομβωτικής αγωγής μετά την τυπική διάρκεια της ΔΑΜΑ. Αυτές οι κατηγορίες περιλαμβάνουν άτομα με σύνθετη στεφανιαία νόσο, σακχαρώδη διαβήτη (ΣΔ), υποτροπιάζον έμφραγμα του μυοκαρδίου, πρώιμη ή επιταχυνόμενη στεφανιαία νόσο, συνοδό περιφερική αρτηριακή νόσο ή συστηματική φλεγμονώδη νόσο(17-18). Επιπλέον, σε αυτές τις συστάσεις λαμβάνονται υπόψη τεχνικές πτυχές όπως η εμφύτευση τουλάχιστον τριών stents, συνολικό μήκος stent 60 mm ή περισσότερο, σύμπλοκη επαναγγείωση ή θρόμβωση stent κατά τη διάρκεια αντιαιμοπεταλιακής θεραπείας.
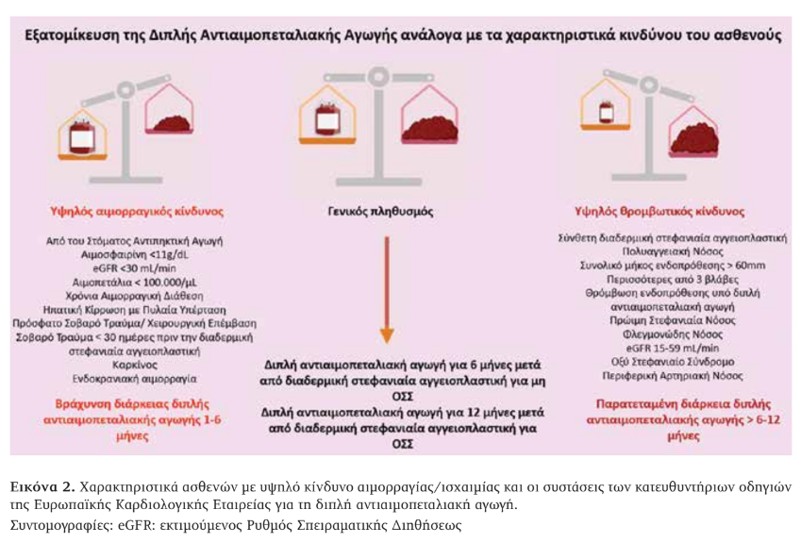
Στην Εικόνα 2 συνοψίζονται τα χαρακτηριστικά των ασθενών με υψηλό κίνδυνο αιμορραγίας ή ισχαιμίας, καθώς και οι συστάσεις των κατευθυντήριων οδηγιών της Ευρωπαϊκής Καρδιολογικής Εταιρείας για τη διάρκεια της διπλής αντιαιμοπεταλιακής αγωγής τόσο στον γενικό πληθυσμό όσο και σε αυτές τις ειδικές ομάδες ασθενών.
Εξατομίκευση της ΔΑΜΑ για συγκεκριμένους πληθυσμούς ασθενών.
A. ΔΑΜΑ μετά από PCI σε ασθενείς με σακχαρώδη διαβήτη.
Περισσότερο από το 30% των ατόμων με διαβήτη παγκοσμίως εμφανίζουν ταυτόχρονα καρδιαγγειακή νόσο, η οποία ευθύνεται για περίπου τους μισούς θανάτους (21). Το φαινόμενο αυτό μπορεί ενδεχομένως να αποδοθεί στην παρουσία πολυεστιακών βλαβών στα στεφανιαία αγγεία, καθώς παρατηρείται συχνά σε αυτούς τους ασθενείς, αλλά και στην αυξημένη ευαισθησία τους στην επαναστένωση του stent (22). Τέλος, στους ασθενείς αυτούς έχει παρατηρηθεί αντίσταση στην αντιαιμοπεταλιακή θεραπεία (23). Σύμφωνα με τις τρέχουσες κατευθυντήριες οδηγίες, η συνιστάμενη διάρκεια ΔΑΜΑ μετά από διαδερμική στεφανιαία παρέμβαση σε διαβητικούς ασθενείς κυμαίνεται από 3 έως 12 μήνες. Ωστόσο, η διάρκεια μπορεί να παραταθεί έως και 30 μήνες με βάση την κλινική κρίση του θεράποντα ιατρού (2-3).
Μια συστηματική ανασκόπηση και μετα-ανάλυση από τους Gargiulo et al. η οποία συμπεριέλαβε 11.473 συμμετέχοντες, διερεύνησε τα κλινικά αποτελέσματα της βραχυπρόθεσμης (≤6 μήνες) έναντι της μακροπρόθεσμης (12 μήνες) διπλής αντιαιμοπεταλιακής αγωγής μετά από PCI σε ασθενείς με και χωρίς διαβήτη. Τα ευρήματα έδειξαν ότι, αν και ο διαβήτης αναγνωρίστηκε ως ανεξάρτητος προγνωστικός παράγοντας μείζονος δυσμενούς καρδιακού συμβάματος (MACE) (HR 2,30, 95% CI 1,01-5,27, P=0,048), η μακροχρόνια ΔΑΜΑ δεν μείωσε τον κίνδυνο MACE, αλλά αντίθετα, αύξησε τον κίνδυνο αιμορραγίας μεταξύ των ασθενών με stent, ανεξάρτητα από την κατάσταση του διαβήτη (24).
Επιπρόσθετα, μια πρόσφατη μετα-ανάλυση που περιελάμβανε 8 μελέτες και 12.665 συμμετέχοντες παρατήρησε ότι η εφαρμογή διπλής αντιαιμοπεταλιακής αγωγής για ≤3 μήνες (S-DAPT) σε διαβητικούς ασθενείς οδήγησε σε 17% μείωση του κινδύνου μείζονων αιμορραγικών και ισχαιμικών συμβαμάτων (NACE) σε σύγκριση με την κλασσική ΔΑΜΑ (RR: 0,83, 95% CI; 0,72-0,96). Τα ευρήματα αυτά υποδηλώνουν ότι η S-DAPT θα μπορούσε να αποτελέσει μια βιώσιμη και ασφαλή θεραπευτική επιλογή για τους διαβητικούς ασθενείς. Επιπλέον, είναι ενδιαφέρον ότι η ανάλυση έδειξε ότι η S-DAPT με βάση την τικαγρελόρη συνδέεται με μειωμένα ποσοστά θνησιμότητας (25).
Αντιθέτως, οι Grodzinsky et al. διεξήγαγαν μια μελέτη που περιλάμβανε 2334 ασθενείς από 10 νοσοκομεία των ΗΠΑ, εστιάζοντας στον κίνδυνο αιμορραγίας σε ασθενείς με ΣΔ, στους οποίους έχει συνταγογραφηθεί ΔΑΜΑ μετά από PCI. Τα ευρήματά, έδειξαν ότι οι διαβητικοί ασθενείς παρουσίασαν λιγότερα αιμορραγικά συμβάματα κατά τη διάρκεια της περιόδου παρακολούθησης 1 έτους μετά την ΔΑΜΑ (RR 0,89, 95% CI 0,83-0,96) σε σύγκριση με τους μη διαβητικούς ασθενείς. Κατά συνέπεια, κατέληξαν στο συμπέρασμα ότι η παράταση της διπλής αντιαιμοπεταλιακής αγωγής μπορεί να είναι επωφελής για τους διαβητικούς ασθενείς, δεδομένου του αυξημένου ισχαιμικού κίνδυνου που διατρέχουν (26).
B. ΔΑΜΑ μετά από σύμπλοκη PCI
Η σύμπλοκη PCI, αναφέρεται σε διαδικασίες διαδερμικής στεφανιαίας παρέμβασης που περιλαμβάνουν δύσκολα ανατομικά χαρακτηριστικά, όπως πολλαπλές ή έντονα ασβεστοποιημένες βλάβες, χρόνιες ολικές αποφράξεις, βλάβες διχάσμου ή βλάβες σε μικρά αγγεία. Αυτές οι συμπλοκες επεμβάσεις αποτελούν περισσότερο από το 30% των συνολικών επεμβάσεων PCI και συχνά απαιτούν προηγμένες τεχνικές και εξειδικευμένο εξοπλισμό για την επίτευξη επιτυχημένων αποτελεσμάτων. Για το λόγο αυτό, οι ασθενείς που υποβάλλονται σε σύμπλοκη PCI αντιμετωπίζουν αυξημένη πιθανότητα εμφάνισης ανεπιθύμητων συμβαμάτων, όπως θνησιμότητα, έμφραγμα του μυοκαρδίου και θρόμβωση του stent. Ως εκ τούτου, η επακόλουθη αντιθρομβωτική θεραπεία διαδραματίζει σημαντικό ρόλο στη άμβλυνση αυτών των κινδύνων (27-28).
Οι Angelo et al. διεξήγαγαν μια μετα-ανάλυση που περιελάμβανε 31.627 ασθενείς από 5 μελέτες, εκ των οποίων οι 8.328 (26,3%) υποβλήθηκαν σε σύμπλοκη PCI. Η μελέτη είχε ως στόχο να αξιολογήσει την αποτελεσματικότητα και την ασφάλεια της βραχείας ΔΑΜΑ (1-3 μήνες) σε σύγκριση με την τυπική ΔΑΜΑ (≥12 μήνες) με βάση την πολυπλοκότητα της PCI. Οι συγγραφείς κατέληξαν στο συμπέρασμα ότι οι ασθενείς που υποβάλλονται σε σύμπλοκη PCI μπορεί να έχουν μεγαλύτερο όφελος και λιγότερες ανεπιθύμητες ενέργειες από τη μονοθεραπεία με αναστολέα P2Y12 μετά την πρώιμη διακοπή της ασπιρίνης σε σύγκριση με την τυπική ΔΑΜΑ. Διαπίστωσαν ότι η μονοθεραπεία με αναστολέα P2Y12, σε σύγκριση με την τυπική ΔΑΜΑ, συσχετίστηκε με παρόμοια αποτελέσματα θνητότητας από όλες τις αιτίες, θρόμβωσης stent και εγκεφαλικού επεισοδίου, χωρίς να παρατηρηθεί αλληλεπίδραση μεταξύ σύμπλοκης και μη σύμπλοκης PCI. Ωστόσο, σημείωσαν μειωμένο κίνδυνο εμφράγματος του μυοκαρδίου στην σύμπλοκη PCI (HR 0,77, 95% CI 0,60-0,99, P = 0,042), καθώς και σημαντικά μειωμένη επίπτωση μείζονος αιμορραγίας (HR 0,67, 95% CI 0,49-0,91, P = 0,010) με τη στρατηγική της σύντομης ΔΑΜΑ (29).
Επιπλέον, οι Apostolos et al. διεξήγαγαν μια άλλη πρόσφατη μετα-ανάλυση που περιελάμβανε 6275 άτομα για να διερευνήσουν την ασφάλεια και την αποτελεσματικότητα ενός σχήματος ΔΑΜΑ διάρκειας ενός μηνός σε σύγκριση με μεγαλύτερη διάρκεια μετά από σύμπλοκη PCI. Η μελέτη διαπίστωσε ότι η σύντμηση της ΔΑΜΑ σε 30 ημέρες μετά από σύμπλοκη PCI δεν οδήγησε σε αυξημένο κίνδυνο μείζονων αιμορραγικών και ισχαιμικών συμβαμάτων (OR: 0,77, 95% CI: 0,52-1,14) ή μείζονων δυσμενών καρδιακών συμβάντων (συμπεριλαμβανομένης της θνησιμότητας, των εμφραγμάτων του μυοκαρδίου, του εγκεφαλικού επεισοδίου ή της θρόμβωσης του στεντ). Επιπλέον, αν και υπήρξε μείωση της επίπτωσης μείζονος αιμορραγίας, το εύρημα αυτό δεν έφτασε σε στατιστική σημαντικότητα (30).
Η συσχέτιση μεταξύ της συντομευμένης διπλής αντιαιμοπεταλιακής θεραπείας και της μειωμένης επίπτωσης μείζονων αιμορραγικών επεισοδίων, χωρίς αντίστοιχη αύξηση της θνησιμότητας ή των ισχαιμικών επεισοδίων, ενισχύεται από τις εξελίξεις της βιοτεχνολογίας (13).Αυτές οι εξελίξεις περιλαμβάνουν την ανάπτυξη των Drug Eluting Stents (DES), τα οποία έχουν εγκριθεί για τη συντόμευση της ΔΑΜΑ σε 1 μήνα. Επιπλέον, η αυξανόμενη χρήση και η πρόοδος στις τεχνικές ενδοαγγειακής απεικόνισης, όπως ο ενδοαγγειακός υπέρηχος (IVUS) και η οπτική τομογραφία συνοχής (OCT), έχουν συμβάλλει στη βελτιστοποίηση των διαδικασιών διαδερμικής στεφανιαίας παρέμβασης (31). Επομένως, ακόμη και σε περιπτώσεις υψηλής πολυπλοκότητας PCI, η σύντμηση της ΔΑΜΑ μπορεί να είναι ασφαλής.
C. DAPT μετά από PCI σε ασθενείς με κακοήθειες.
Οι ασθενείς που λαμβάνουν διπλή αντιαιμοπεταλιακή θεραπεία για CAD και έχουν επίσης συνυπάρχουσα κακοήθεια αποτελούν μια υποομάδα ατόμων με αυξημένο κίνδυνο τόσο αιμορραγίας όσο και ισχαιμίας. Αυτή η υποομάδα, η οποία εκτιμάται ότι φτάνει έως και το 15% των ασθενών με οξύ στεφανιαίο σύνδρομο, προσθέτει περαιτέρω πολυπλοκότητα στη φαρμακολογική διαχείριση μετά από PCI (32).
Μελέτες έχουν δείξει ότι οι επανεισαγωγές λόγω οξέος εμφράγματος του μυοκαρδίου εντός 90 ημερών μετά την PCI είναι συχνότερες σε ασθενείς με συνυπάρχουσες κακοήθειες (12,1% στον πνεύμονα, 10,8% στο παχύ έντερο, 7,5% στο μαστό, 7,0% στον προστάτη και 9,1% συνολικά). Ομοίως, το ποσοστό επανανοσηλείας λόγω αιμορραγίας είναι επίσης αυξημένο (4,2% στο παχύ έντερο, 1,5% στον πνεύμονα, 1,4% στον προστάτη, 0,6% στο μαστό και 1,6% συνολικά) (33). Τα ποσοστά αυτά μπορούν να αποδοθούν στο γεγονός ότι οι ασθενείς με κακοήθεια έχουν πολλά σύνθετα χαρακτηριστικά. Εκτός από τις συνήθεις ανεπιθύμητες ενέργειες που σχετίζονται με την κακοήθεια, όπως η υπερπηκτικότητα και η αναιμία, η χημειοθεραπεία και η ακτινοθεραπεία μπορεί να προκαλέσουν προθρομβωτικές, αγγειοσυσπαστικές και προφλεγμονώδεις επιδράσεις στο αγγειακό σύστημα. Επιπλέον, το ενδεχόμενο υποτροπής, μπορεί να καταστήσει αναγκαία τη διακοπή της ΔΑΜΑ για διαδικασίες όπως βιοψίες, χειρουργικές επεμβάσεις ή επανέναρξη της αντικαρκινικής αγωγής (34-35).
Σύμφωνα με τις κατευθυντήριες οδηγίες της ESC για την καρδιο-ογκολογία του 2022, η διάρκεια της ΔΑΜΑ θα πρέπει να είναι όσο το δυνατόν συντομότερη, ενώ ως βέλτιστο θεραπευτικό σχήμα προτείνεται η ΔΑΜΑ με βάση την κλοπιδογρέλη για 1-3 μήνες σε ασθενείς με αριθμό αιμοπεταλίων άνω των 30.000/μl. Άλλωστε, η Academic Research Consortium for High Bleeding Risk καθιέρωσε πρόσφατα τη διάρκεια της ΔΑΜΑ ενός μηνός ως τη βέλτιστη, μετά την PCI για ασθενείς με ενεργό καρκίνο (εξαιρουμένου του μη μελανωματικού καρκίνου του δέρματος) και υψηλό κίνδυνο αιμορραγίας. Επιπλέον, συνίσταται τρίμηνη διάρκεια της ΔΑΜΑ για ασθενείς με κακοήθεια που θεωρούνται μη υψηλού κινδύνου. Σε περιπτώσεις οξέος στεφανιαίου συνδρόμου με αυξημένο κίνδυνο ισχαιμίας, προτείνεται παράταση της ΔΑΜΑ στους έξι μήνες (36).
Τέλος, η έναρξη της απεικόνισης OCT μπορεί να βοηθήσει στην καθοδήγηση της διακοπής της ΔΑΜΑ. Αυτό οφείλεται στο γεγονός ότι οι παράγοντες κινδύνου για θρόμβωση του stent, όπως η κακή θέση, η ατελής κάλυψη του στόχου και η επαναστένωση του αυλού, μπορεί να απεικονιστούν. Κατά συνέπεια, μπορούν να εντοπιστούν ασθενείς χαμηλού κινδύνου που δύνανται να διακόψουν με ασφάλεια την ΔΑΜΑ και να προχωρήσουν σε βασικές χειρουργικές επεμβάσεις ή άλλες θεραπευτικές διαδικασίες που σχετίζονται με την κακοήθεια (37).
Συνολικά, σε αυτόν τον ευάλωτο πληθυσμό ασθενών, μια εξατομικευμένη και διεπιστημονική προσέγγιση είναι υψίστης σημασίας για τη βελτίωση τόσο του προσδόκιμου όσο και της ποιότητας ζωής των ασθενών.
Μελλοντικές προοπτικές
Η βέλτιστη διάρκεια της διπλής αντιαιμοπεταλιακής θεραπείας και η αποτελεσματικότερη φαρμακευτική στρατηγική για την επακόλουθη μονοθεραπεία αποτέλεσαν αντικείμενο πρόσφατης εξέτασης σε κλινικές μελέτες. Μετά τα ενθαρρυντικά αποτελέσματα από μελέτες που συνηγορούν υπέρ της μειωμένης διάρκειας της ΔΑΜΑ, με επακόλουθη χορήγηση ενός αναστολέα P2Y12 μόνο, έχει αυξηθεί το ενδιαφέρον για τη διερεύνηση της πλήρους απόσυρσης της ασπιρίνης αμέσως μετά τη διαδερμική στεφανιαία παρέμβαση. Η πρόσφατη μελέτη ASET (38), μια πιλοτική έρευνα που διεξήχθη από τους Kogame et al. εξέτασε την ασφάλεια και την αποτελεσματικότητα της μονοθεραπείας με πρασουγρέλη μετά την επιτυχή εμφύτευση stent με χρήση everolimus σε μια επιλεγμένη ομάδα ασθενών με χαμηλή ανατομική πολυπλοκότητα και σταθερή στεφανιαία νόσο. Η μελέτη απέδωσε θετικά αποτελέσματα, γεγονός που προκάλεσε την έναρξη μεγαλύτερων RCTs για την περαιτέρω αξιολόγηση αυτής της θεραπευτικής προσέγγισης. Επιπλέον, πρόσφατα δημοσιεύθηκε η πολυαναμενόμενη μελέτη STOP-DAPT-3 (39), η οποία συνέκρινε τη χορήγηση μίας μόνο χαμηλής δόσης πρασουγρέλης με τη συνήθη στρατηγική ΔΑΜΑ σε ασθενείς μετά από PCI μετά από οξύ στεφανιαίο σύνδρομο ή σε ασθενείς με υψηλό κίνδυνο αιμορραγίας. Ωστόσο, η στρατηγική της δοκιμής χωρίς ασπιρίνη απέτυχε να μειώσει τη μείζονα αιμορραγία εντός 1 μηνός και έδειξε αυξημένο κίνδυνο στεφανιαίων επεισοδίων. Κατά συνέπεια, η εν εξελίξει μελέτη NEO-MINDSET (NCT04360720) υπόσχεται να δώσει περισσότερες πληροφορίες σχετικά με αυτή την καινοτόμο στρατηγική και να διευκρινίσει τις δυνατότητες εφαρμογής της στην κλινική πράξη (40). Σημαντική επανάσταση στον τομέα της ΔΑΜΑ μπορεί να φέρει η εισαγωγή πολλών νέων αντιαιμοπεταλιακών παραγόντων. Μεταξύ αυτών των παραγόντων που βρίσκονται υπό διερεύνηση για χρήση σε ασθενείς που υποβάλλονται σε PCI είναι η σελατογρέλη, ένας αναστρέψιμος ανταγωνιστής του υποδοχέα P2Y12 μη-θειενοπυριδίνης που χορηγείται υποδόρια (41), καθώς και το revacept, ένας ενδοφλεβίως χορηγούμενος αναστολέας του GPVI, του κύριου υποδοχέα κολλαγόνου των αιμοπεταλίων (42)– και το RUC-4, ένας αναστολέας GPIIb/IIIa με νέο μηχανισμό δράσης που έχει σχεδιαστεί για ενδομυϊκή χορήγηση (43). Αυτοί οι καινοτόμοι αντιαιμοπεταλιακοί παράγοντες υπόσχονται πολλά για τη βελτίωση των αποτελεσμάτων και τη μείωση των επιπλοκών σε ασθενείς που υποβάλλονται σε PCI.
Συμπέρασμα
Εν κατακλείδι, το μέλλον της ΔΑΜΑ έγκειται στη συνεχή εξέλιξή της, με γνώμονα την πρόοδο της ιατρικής επιστήμης και της τεχνολογίας, καθώς και τη βαθύτερη κατανόηση των ειδικών παραγόντων για τον κάθε ασθενή. Με την εφαρμογή τεκμηριωμένων προσεγγίσεων και την καινοτομία, οι κλινικοί ιατροί μπορούν να βελτιστοποιήσουν τις στρατηγικές θεραπείας και τελικά να βελτιώσουν την πρόγνωση και την ποιότητα ζωής των ασθενών που υποβάλλονται σε PCI.
1. Hudzik B, Błachut A, Lesiak M, Kubica J, Wojakowski W, Gąsior M. Summary of the European Society of Cardiology guidelines on dual antiplatelet therapy in patients after percutaneous coronary interventions. Kardiol Pol. 2022;80(10):974-989.
2. Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, Claeys MJ, Dan GA, Dweck MR, Galbraith M, Gilard M, Hinterbuchner L, Jankowska EA, Jüni P, Kimura T, Kunadian V, Leosdottir M, Lorusso R, Pedretti RFE, Rigopoulos AG, Rubini Gimenez M, Thiele H, Vranckx P, Wassmann S, Wenger NK, Ibanez B; ESC Scientific Document Group. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44(38):3720-3826.
3. Knuuti J, Wijns W, Saraste A, Capodanno D, Barbato E, Funck-Brentano C, Prescott E, Storey RF, Deaton C, Cuisset T, Agewall S, Dickstein K, Edvardsen T, Escaned J, Gersh BJ, Svitil P, Gilard M, Hasdai D, Hatala R, Mahfoud F, Masip J, Muneretto C, Valgimigli M, Achenbach S, Bax JJ; 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41(3):407-477.
4. Aslam Zahid MB, Memon MS, Tappiti M, Shantha Kumar V, Nazir AM, Koganti B, Gupta K, Mostafa JA. Duration of Dual Antiplatelet Therapy After Stent Implantation, Still an Enigma: A Systematic Review of Randomized Clinical Trials. Cureus. 2021;13(11): e19549
5. Capodanno D, Bhatt DL, Gibson CM, James S, Kimura T, Mehran R, Rao SV, Steg PG, Urban P, Valgimigli M, Windecker S, Angiolillo DJ. Bleeding avoidance strategies in percutaneous coronary intervention. Nat Rev Cardiol. 2022;19(2):117-132.
6. Angiolillo DJ, Galli M, Collet JP, Kastrati A, O’Donoghue ML. Antiplatelet therapy after percutaneous coronary intervention. EuroIntervention. 2022;17(17):e1371-e1396.
7. Kosobucka A, Michalski P, Pietrzykowski Ł, Kasprzak M, Obońska K, Fabiszak T, Felsmann M, Kubica A. Adherence to treatment assessed with the Adherence in Chronic Diseases Scale in patients after myocardial infarction. Patient Prefer Adherence. 2018;12:333-340.
8. Kubica A, Obońska K, Kasprzak M, Sztuba B, Navarese EP, Koziński M, Świątkiewicz I, Kieszkowska M, Ostrowska M, Grześk G, Kubica J. Prediction of high risk of non-adherence to antiplatelet treatment. Kardiol Pol. 2016;74(1):61-7.
9. De Servi S, Roncella A, Reimers B. Causes and clinical implications of premature discontinuation of dual antiplatelet therapy. Curr Opin Cardiol. 2011;26 Suppl 1:S15-21.
10. Zanchin T, Temperli F, Karagiannis A, Zanchin C, Räsänen M, Koskinas KC, Stortecky S, Hunziker L, Praz F, Blöchlinger S, Moro C, Moschovitis A, Seiler C, Billinger M, Heg D, Pilgrim T, Valgimigli M, Windecker S, Räber L. Frequency, Reasons, and Impact of Premature Ticagrelor Discontinuation in Patients Undergoing Coronary Revascularization in Routine Clinical Practice: Results From the Bern Percutaneous Coronary Intervention Registry. Circ Cardiovasc Interv. 2018;11(5):e006132.
11. Frazier SC. Health outcomes and polypharmacy in elderly individuals: an integrated literature review. J Gerontol Nurs. 2005;31(9):4-11.
12. Johansson T, Abuzahra ME, Keller S, Mann E, Faller B, Sommerauer C, Höck J, Löffler C, Köchling A, Schuler J, Flamm M, Sönnichsen A. Impact of strategies to reduce polypharmacy on clinically relevant endpoints: a systematic review and meta-analysis. Br J Clin Pharmacol. 2016;82(2):532-48.
13. Apostolos A, Vasilagkos G, Toutouzas K, Tsigkas G. DAPT Shortening After Complex PCI: Examining the Fine Print. J Am Coll Cardiol. 2023;81(22):e191.
14. Rout A, Sharma A, Ikram S, Garg A. Short-term dual antiplatelet therapy for 1-3 months after percutaneous coronary intervention using drug eluting stents: A systematic review and meta-analysis of randomized clinical trials. Catheter Cardiovasc Interv. 2022
15. Park DY, An S, Kumar A, Malhotra S, Jolly N, Kaur A, Kattoor A, Doukky R, Kalra A, Vij A. Abbreviated versus Standard Duration of DAPT after PCI: A Systematic Review and Network Meta-analysis. Am J Cardiovasc Drugs. 2022;22(6):633-645.
16. Tsigkas G, Apostolos A, Chlorogiannis DD, Bousoula E, Vasilagkos G, Tsalamandris S, Tsiafoutis I, Katsanos K, Toutouzas K, Aminian A, Alexopoulos D, Davlouros P. Thirty-Days versus Longer Duration of Dual Antiplatelet Treatment after Percutaneous Coronary Interventions with Newer Drug-Eluting Stents: A Systematic Review and Meta-Analysis. Life (Basel). 2023;13(3):666.
17. Ueki Y, Bär S, Losdat S, Otsuka T, Zanchin C, Zanchin T, Gragnano F, Gargiulo G, Siontis GCM, Praz F, Lanz J, Hunziker L, Stortecky S, Pilgrim T, Heg D, Valgimigli M, Windecker S, Räber L. Validation of the Academic Research Consortium for High Bleeding Risk (ARC-HBR) criteria in patients undergoing percutaneous coronary intervention and comparison with contemporary bleeding risk scores. EuroIntervention. 2020;16(5):371-379.
18. Urban P, Mehran R, Colleran R, Angiolillo DJ, Byrne RA, Capodanno D, Cuisset T, Cutlip D, Eerdmans P, Eikelboom J, Farb A, Gibson CM, Gregson J, Haude M, James SK, Kim HS, Kimura T, Konishi A, Laschinger J, Leon MB, Magee PFA, Mitsutake Y, Mylotte D, Pocock S, Price MJ, Rao SV, Spitzer E, Stockbridge N, Valgimigli M, Varenne O, Windhoevel U, Yeh RW, Krucoff MW, Morice MC. Defining high bleeding risk in patients undergoing percutaneous coronary intervention: a consensus document from the Academic Research Consortium for High Bleeding Risk. Eur Heart J. 2019;40(31):2632-2653.
19. Capodanno D, Greco A. Dual antiplatelet therapy in patients at high bleeding risk: less is more-more or less. Eur Heart J. 2023 Mar;44(11):969-971.
20. Costa F, Montalto C, Branca M, Hong SJ, Watanabe H, Franzone A, Vranckx P, Hahn JY, Gwon HC, Feres F, Jang Y, De Luca G, Kedhi E, Cao D, Steg PG, Bhatt DL, Stone GW, Micari A, Windecker S, Kimura T, Hong MK, Mehran R, Valgimigli M. Dual antiplatelet therapy duration after percutaneous coronary intervention in high bleeding risk: a meta-analysis of randomized trials. Eur Heart J. 2023;44(11):954-968.
21. Einarson TR, Acs A, Ludwig C, Panton UH. Prevalence of cardiovascular disease in type 2 diabetes: a systematic literature review of scientific evidence from across the world in 2007-2017. Cardiovasc Diabetol. 2018;17(1):83.
22. Wilson S, Mone P, Kansakar U, Jankauskas SS, Donkor K, Adebayo A, Varzideh F, Eacobacci M, Gambardella J, Lombardi A, Santulli G. Diabetes and restenosis. Cardiovasc Diabetol. 2022;21(1):23.
23. Ajjan R, Storey RF, Grant PJ. Aspirin resistance and diabetes mellitus. Diabetologia. 2008;51(3):385-390.
24. Gargiulo G, Windecker S, da Costa BR, Feres F, Hong MK, Gilard M, Kim HS, Colombo A, Bhatt DL, Kim BK, Morice MC, Park KW, Chieffo A, Palmerini T, Stone GW, Valgimigli M. Short term versus long term dual antiplatelet therapy after implantation of drug eluting stent in patients with or without diabetes: systematic review and meta-analysis of individual participant data from randomised trials. BMJ. 2016;355:i5483.
25. Apostolos A, Travlos C, Tsioulos G, Chlorogiannis DD, Karanasos A, Papafaklis M, Alexopoulos D, Toutouzas K, Davlouros P, Tsigkas G. Duration of Dual Antiplatelet Treatment After Percutaneous Coronary Intervention in Patients With Diabetes: A Systematic Review and Meta-analysis. J Cardiovasc Pharmacol. 2024;83(1):64-72.
26. Grodzinsky A, Arnold SV, Wang TY, Sharma P, Gosch K, Jones PG, Bhatt DL, Steg PG, McGuire DK, Cohen DJ, Spertus JA, Chhatriwalla AK, Lind M, Graham G, Kosiborod M. Bleeding risk following percutaneous coronary intervention in patients with diabetes prescribed dual anti-platelet therapy. Am Heart J. 2016;182:111-118.
27. Iftikhar SF, Bishop MA, Hu P. Complex Coronary Artery Lesions. StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024
28. Valgimigli M, Bueno H, Byrne RA, Collet JP, Costa F, Jeppsson A, Jüni P, Kastrati A, Kolh P, Mauri L, Montalescot G, Neumann FJ, Petricevic M, Roffi M, Steg PG, Windecker S, Zamorano JL, Levine GN; 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2018;53(1):34-78.
29. Oliva A, Castiello DS, Franzone A, Condorelli G, Colombo A, Esposito G, Stefanini GG, Piccolo R. P2Y12 Inhibitors Monotherapy in Patients Undergoing Complex vs Non-Complex Percutaneous Coronary Intervention: A Meta-Analysis of Randomized Trials. Am Heart J. 2023;255:71-81.
30. Apostolos, A.; Chlorogiannis, D.-D.; Chrysostomidis, G.; Bozika, M.; Timpilis, F.; Kramvis, A.; Karamasis, G.V.; Leventopoulos, G.; Davlouros, P.; Tsigkas, G. Efficacy and Safety of Thirty-Day Dual-Antiplatelet Therapy Following Complex Percutaneous Coronary Intervention: A Systematic Review and Meta-Analysis. J. Cardiovasc. Dev. Dis. 2024;11(2): 43
31. Apostolos A, Chlorogiannis D, Vasilagkos G, Katsanos K, Toutouzas K, Aminian A, Alexopoulos D, Davlouros P, Tsigkas G. Safety and efficacy of shortened dual antiplatelet therapy after complex percutaneous coronary intervention: A systematic review and meta- analysis. Hellenic J Cardiol. 2023;71:33-41.
32. Radmilovic J, Di Vilio A, D'Andrea A, Pastore F, Forni A, Desiderio A, Ragni M, Quaranta G, Cimmino G, Russo V, Scherillo M, Golino P. The Pharmacological Approach to Oncologic Patients with Acute Coronary Syndrome. J Clin Med. 2020;9(12):3926.
33. Kwok CS, Wong CW, Kontopantelis E, Barac A, Brown SA, Velagapudi P, Hilliard AA, Bharadwaj AS, Chadi Alraies M, Mohamed M, Bhatt DL, Mamas MA. Percutaneous coronary intervention in patients with cancer and readmissions within 90 days for acute myocardial infarction and bleeding in the USA. Eur Heart J. 2021;42(10):1019-1034.
34. Falanga A, Marchetti M, Vignoli A. Coagulation and cancer: biological and clinical aspects. J Thromb Haemost. 2013;11(2):223-33.
35. de Boer RA, Meijers WC, van der Meer P, van Veldhuisen DJ. Cancer and heart disease: associations and relations. Eur J Heart Fail. 2019;21(12):1515-1525.
36. Tsigkas G, Vakka A, Apostolos A, Bousoula E, Vythoulkas-Biotis N, Koufou EE, Vasilagkos G, Tsiafoutis I, Hamilos M, Aminian A, Davlouros P. Dual Antiplatelet Therapy and Cancer; Balancing between Ischemic and Bleeding Risk: A Narrative Review. J Cardiovasc Dev Dis. 2023;10(4):135.
37. Iliescu CA, Cilingiroglu M, Giza DE, Rosales O, Lebeau J, Guerrero-Mantilla I, Lopez- Mattei J, Song J, Silva G, Loyalka P, Paixao ARM, Yusuf SW, Perin E, Anderson VH, Marmagkiolis K. "Bringing on the light" in a complex clinical scenario: Optical coherence tomography-guided discontinuation of antiplatelet therapy in cancer patients with coronary artery disease (PROTECT-OCT registry). Am Heart J. 2017;194:83-91.
38. Kogame N, Guimarães PO, Modolo R, De Martino F, Tinoco J, Ribeiro EE, Kawashima H, Ono M, Hara H, Wang R, Cavalcante R, Moulin B, Falcão BAA, Leite RS, de Almeida Sampaio FB, Morais GR, Meireles GC, Campos CM, Onuma Y, Serruys PW, Lemos PA. Aspirin-Free Prasugrel Monotherapy Following Coronary Artery Stenting in Patients With Stable CAD: The ASET Pilot Study. JACC Cardiovasc Interv. 2020;13(19):2251-2262.
39. Natsuaki M, Watanabe H, Morimoto T, Yamamoto K, Obayashi Y, Nishikawa R, Ando K, Domei T, Suwa S, Ogita M, Isawa T, Takenaka H, Yamamoto T, Ishikawa T, Hisauchi I, Wakabayashi K, Onishi Y, Hibi K, Kawai K, Yoshida R, Suzuki H, Nakazawa G, Kusuyama T, Morishima I, Ono K, Kimura T. An Aspirin-Free Versus Dual Antiplatelet Strategy for Coronary Stenting: STOPDAPT-3 Randomized Trial. Circulation. 2023;149:585–600
40. ClinicalTrials.gov Identifier: NCT04360720: «PercutaNEOus Coronary Intervention Followed by Monotherapy INstead of Dual Antiplatelet Therapy in the SETting of Acute Coronary Syndromes: The NEO-MINDSET Trial (NEOMINDSET)»
41. Beavers CJ, Effoe SA, Dobesh PP. Selatogrel: A Novel Subcutaneous P2Y12 Inhibitor. J Cardiovasc Pharmacol. 2022;79(2):161-167.
42. Mayer K, Hein-Rothweiler R, Schüpke S, Janisch M, Bernlochner I, Ndrepepa G, Sibbing D, Gori T, Borst O, Holdenrieder S, Kupka D, Petzold T, Bradaric C, Okrojek R, Leistner DM, Trippel TD, Münzel T, Landmesser U, Pieske B, Zeiher AM, Gawaz MP, Hapfelmeier A, Laugwitz KL, Schunkert H, Kastrati A, Massberg S. Efficacy and Safety of Revacept, a Novel Lesion-Directed Competitive Antagonist to Platelet Glycoprotein VI, in Patients Undergoing Elective Percutaneous Coronary Intervention for Stable Ischemic Heart Disease: The Randomized, Double-blind, Placebo Controlled ISAR-PLASTER Phase 2 Trial. JAMA Cardiol. 2021;6(7):753-761.
43. Li J, Vootukuri S, Shang Y, Negri A, Jiang JK, Nedelman M, Diacovo TG, Filizola M, Thomas CJ, Coller BS. RUC-4: a novel αIIbβ3 antagonist for prehospital therapy of myocardial infarction. Arterioscler Thromb Vasc Biol. 2014;34(10):2321-2329.
44. Hong SJ, Kim JS, Hong SJ, Lim DS, Lee SY, Yun KH, Park JK, Kang WC, Kim YH, Yoon HJ, Won H, Nam CM, Ahn CM, Kim BK, Ko YG, Choi D, Jang Y, Hong MK; One-Month DAPT Investigators. 1-Month Dual-Antiplatelet Therapy Followed by Aspirin Monotherapy After Polymer-Free Drug-Coated Stent Implantation: One-Month DAPT Trial. JACC Cardiovasc Interv. 2021;14(16):1801-1811.
45. De Luca G, Damen SA, Camaro C, Benit E, Verdoia M, Rasoul S, Liew HB, Polad J, Ahmad WA, Zambahari R, Postma S, Kedhi E, Suryapranata H; Collaborators. Final results of the randomised evaluation of short-term dual antiplatelet therapy in patients with acute coronary syndrome treated with a new-generation stent (REDUCE trial). EuroIntervention. 2019;15(11):e990-e998.
46. Kim BK, Hong SJ, Cho YH, Yun KH, Kim YH, Suh Y, Cho JY, Her AY, Cho S, Jeon DW, Yoo SY, Cho DK, Hong BK, Kwon H, Ahn CM, Shin DH, Nam CM, Kim JS, Ko YG, Choi D, Hong MK, Jang Y; TICO Investigators. Effect of Ticagrelor Monotherapy vs Ticagrelor With Aspirin on Major Bleeding and Cardiovascular Events in Patients With Acute Coronary Syndrome: The TICO Randomized Clinical Trial. JAMA. 2020;323(23):2407-2416.
47. Mehran R, Baber U, Sharma SK, Cohen DJ, Angiolillo DJ, Briguori C, Cha JY, Collier T, Dangas G, Dudek D, Džavík V, Escaned J, Gil R, Gurbel P, Hamm CW, Henry T, Huber K, Kastrati A, Kaul U, Kornowski R, Krucoff M, Kunadian V, Marx SO, Mehta SR, Moliterno D, Ohman EM, Oldroyd K, Sardella G, Sartori S, Shlofmitz R, Steg PG, Weisz G, Witzenbichler B, Han YL, Pocock S, Gibson CM. Ticagrelor with or without Aspirin in High-Risk Patients after PCI. N Engl J Med. 2019;381(21):2032-2042.
48. Valgimigli M, Frigoli E, Heg D, Tijssen J, Jüni P, Vranckx P, Ozaki Y, Morice MC, Chevalier B, Onuma Y, Windecker S, Tonino PAL, Roffi M, Lesiak M, Mahfoud F, Bartunek J, Hildick-Smith D, Colombo A, Stanković G, Iñiguez A, Schultz C, Kornowski R, Ong PJL, Alasnag M, Rodriguez AE, Moschovitis A, Laanmets P, Donahue M, Leonardi S, Smits PC; MASTER DAPT Investigators. Dual Antiplatelet Therapy after PCI in Patients at High Bleeding Risk. N Engl J Med. 2021;385(18):1643-1655.
49. Hahn JY, Song YB, Oh JH, Chun WJ, Park YH, Jang WJ, Im ES, Jeong JO, Cho BR, Oh SK, Yun KH, Cho DK, Lee JY, Koh YY, Bae JW, Choi JW, Lee WS, Yoon HJ, Lee SU, Cho JH, Choi WG, Rha SW, Lee JM, Park TK, Yang JH, Choi JH, Choi SH, Lee SH, Gwon HC; SMART- CHOICE Investigators. Effect of P2Y12 Inhibitor Monotherapy vs Dual Antiplatelet Therapy on Cardiovascular Events in Patients Undergoing Percutaneous Coronary Intervention: The SMART-CHOICE Randomized Clinical Trial. JAMA. 2019;321(24):2428-2437.
50. Vranckx P, Valgimigli M, Jüni P, Hamm C, Steg PG, Heg D, van Es GA, McFadden EP, Onuma Y, van Meijeren C, Chichareon P, Benit E, Möllmann H, Janssens L, Ferrario M, Moschovitis A, Zurakowski A, Dominici M, Van Geuns RJ, Huber K, Slagboom T, Serruys PW, Windecker S; GLOBAL LEADERS Investigators. Ticagrelor plus aspirin for 1 month, followed by ticagrelor monotherapy for 23 months vs aspirin plus clopidogrel or ticagrelor for 12 months, followed by aspirin monotherapy for 12 months after implantation of a drug-eluting stent: a multicentre, open-label, randomised superiority trial. Lancet. 2018;392(10151):940-949.
51. Watanabe H, Morimoto T, Natsuaki M, Yamamoto K, Obayashi Y, Ogita M, Suwa S, Isawa T, Domei T, Yamaji K, Tatsushima S, Watanabe H, Ohya M, Tokuyama H, Tada T, Sakamoto H, Mori H, Suzuki H, Nishikura T, Wakabayashi K, Hibi K, Abe M, Kawai K, Nakao K, Ando K, Tanabe K, Ikari Y, Morino Y, Kadota K, Furukawa Y, Nakagawa Y, Kimura T; STOPDAPT-2 ACS Investigators. Comparison of Clopidogrel Monotherapy After 1 to 2 Months of Dual Antiplatelet Therapy With 12 Months of Dual Antiplatelet Therapy in Patients With Acute Coronary Syndrome: The STOPDAPT-2 ACS Randomized Clinical Trial. JAMA Cardiol. 2022;7(4):407-417.
52. Watanabe H, Morimoto T, Natsuaki M, Yamamoto K, Obayashi Y, Nishikawa R, Ando K, Ono K, Kadota K, Suwa S, Morishima I, Yoshida R, Hata Y, Akao M, Yagi M, Suematsu N, Morino Y, Yokomatsu T, Takamisawa I, Noda T, Doi M, Okayama H, Nakamura Y, Hibi K, Sakamoto H, Noguchi T, Kimura T; STOPDAPT-2 Investigators. Clopidogrel vs Aspirin Monotherapy Beyond 1 Year After Percutaneous Coronary Intervention. J Am Coll Cardiol. 2024;83(1):17-31.
53. Franzone A, McFadden E, Leonardi S, Piccolo R, Vranckx P, Serruys PW, Benit E, Liebetrau C, Janssens L, Ferrario M, Zurakowski A, Diletti R, Dominici M, Huber K, Slagboom T, Buszman P, Bolognese L, Tumscitz C, Bryniarski K, Aminian A, Vrolix M, Petrov I, Garg S, Naber C, Prokopczuk J, Hamm C, Steg PG, Heg D, Jüni P, Windecker S, Valgimigli M; GLASSY Investigators. Ticagrelor Alone Versus Dual Antiplatelet Therapy From 1 Month After Drug- Eluting Coronary Stenting. J Am Coll Cardiol. 2019;74(18):2223-2234.
54. Baber U, Dangas G, Angiolillo DJ, Cohen DJ, Sharma SK, Nicolas J, Briguori C, Cha JY, Collier T, Dudek D, Džavik V, Escaned J, Gil R, Gurbel P, Hamm CW, Henry T, Huber K, Kastrati A, Kaul U, Kornowski R, Krucoff M, Kunadian V, Marx SO, Mehta S, Moliterno D, Ohman EM, Oldroyd K, Sardella G, Sartori S, Shlofmitz R, Steg PG, Weisz G, Witzenbichler B, Han YL, Pocock S, Gibson CM, Mehran R. Ticagrelor alone vs. ticagrelor plus aspirin following percutaneous coronary intervention in patients with non-ST-segment elevation acute coronary syndromes: TWILIGHT-ACS. Eur Heart J. 2020;41(37):3533-3545.
55. van Geuns RJ, Chun-Chin C, McEntegart MB, Merkulov E, Kretov E, Lesiak M, O'Kane P, Hanratty CG, Bressollette E, Silvestri M, Wlodarczak A, Barragan P, Anderson R, Protopopov A, Peace A, Menown I, Rocchiccioli P, Onuma Y, Oldroyd KG. Bioabsorbable polymer drug-eluting stents with 4-month dual antiplatelet therapy versus durable polymer drug-eluting stents with 12-month dual antiplatelet therapy in patients with left main coronary artery disease: the IDEAL-LM randomised trial. EuroIntervention. 2022;17(18):1467-1476.
56. Escaned J, Cao D, Baber U, Nicolas J, Sartori S, Zhang Z, Dangas G, Angiolillo DJ, Briguori C, Cohen DJ, Collier T, Dudek D, Gibson M, Gil R, Huber K, Kaul U, Kornowski R, Krucoff MW, Kunadian V, Mehta S, Moliterno DJ, Ohman EM, Oldroyd KG, Sardella G, Sharma SK, Shlofmitz R, Weisz G, Witzenbichler B, Pocock S, Mehran R. Ticagrelor monotherapy in patients at high bleeding risk undergoing percutaneous coronary intervention: TWILIGHT-HBR. Eur Heart J. 2021;42(45):4624-4634.
57. Mehran R, Cao D, Angiolillo DJ, Bangalore S, Bhatt DL, Ge J, Hermiller J, Makkar RR, Neumann FJ, Saito S, Picon H, Toelg R, Maksoud A, Chehab BM, De la Torre Hernandez JM, Kunadian V, Sardella G, Thiele H, Varenne O, Vranckx P, Windecker S, Zhou Y, Krucoff MW, Ruster K, Wang J, Valgimigli M; XIENCE 90 and XIENCE 28 Investigators. 3- or 1-Month DAPT in Patients at High Bleeding Risk Undergoing Everolimus-Eluting Stent Implantation. JACC Cardiovasc Interv. 2021;14(17):1870-1883.